Reaksi Eliminasi
Reaksi eliminasi adalah
suatu jenis reaksi organik dimana dua subtitusi dilepaskan dari sebuah molekul
baik dalam satu atau dua langkah mekanisme. Atau reaksi eliminasi juga dapat
diartikan sebagai pemutusan suatu senyawa membentuk senyawa baru. Reaksi
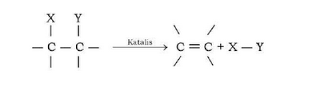
eliminasi dapat dianggap kebalikan dari reaksi adisi. Reaksi ini hanya dapat berlangsung
bila ada zat yang menarik molekul yang akan dieliminasi. Reaksi eliminasi
digunakan untuk membuat senyawa-senyawa alkena dan alkuna.
Reaksi E2
Reaksi E2 (eliminasi
bimolekular) adalah suatu reaksi
eliminasi alkil halida yang paling berguna. Reaksi E2 cenderung
digunakan basa kuat, seperti OH- dan OR-. Reaksi E2
dilangsungkan oleh alkil halida primer dan sekunder. Mekanisme reaksi E2
tidak mengalami karbokation sebagai zat antara seperti yang terjadi direaksi SN1,
melainkan terjadi reaksi serempak yaitu reaksi yang terjadi dalam satu tahap,
sama hal nya yang terjadi pada reaksi SN2.
Mekanisme Reaksi E2
Pertama, basa akan
membentuk ikatan dengan hidrogen. Kedua, elektron-elektron C-H membentuk sebuah
ikatan pi. Kemudian terakhir, Brom bersama sepasang elektronnya meninggalkan ikatan
sigma C-Br.
Tingkat naiknya laju reaksi E2 yaitu
primer, sekunder, tersier. Sama hal nya dalam reaksi SN1, pada reaksi
E2 alkil halida tersier bereaksi paling cepat dan alkil halida primer paling lambat.
PERMASALAHAN
1. Mengapa pada reaksi E2 cenderung
dominan digunakan basa kuat? Jelaskan
2. Bagaimana pengaruh pelarut pada
reaksi E2?
3. Mengapa pada reaksi E2 nukleofil
bertindak sebagai basa?



Hallo ..
BalasHapusSaya Riska dengan Nim (A1C117076) akan membantu menjawab permasalahan nomor 3. Mengapa pada reaksi E2 nukleofil bertindak sebagai basa?
berdasarkan sumber yang telah saya baca, Karena pada Reaksi E2 secara khusus menggunakan basa kuat untuk menarik hidrogen asam dengan kuat. Nukleofil bertindak sebagai basa dan mengambil proton (hidrogen) dari atom karbon yang bersebelahan dengan karbon pembawa gugus pergi. Pada waktu yang bersamaan, gugus pergi terlepas dan ikatan rangkap dua terbentuk.
Saya: MUHAMMAD RIFKY SAIFUDDIN
BalasHapusNIM: A1C117080
Akan menjawab permasalahan no. 2....
Pelarut merupakan salah satu faktor yang dapat mempengaruhi mekanisme reaksi eliminasi E2. Pelarut non polar lebih disukai oleh reaksi ini. Pengaruh pelarut juga dilihat dari kemampuan suatu suatu senyawa untuk mensolvasi ion-ion, karbokation, nukleofil atau basa, dan gugus-gugus pergi. serta menstabilkan ion yang terbentuk atau memberikan kestabilan untuk memudahkan terbentuknya ion-ion molekul.
Nama : Kurnia Aulia
BalasHapusNim : A1C117068
Baiklah disini saya akan mencoba menjawab permasalahan dari lara pada nomor 1
Dimana permasalahannya yaitu mengapa pada reaksi E2 cenderung dominan menggunakan basa kuat?
Disini saya akan membantu menjawab,
Jawaban saya sebenarnya sudah dijawab dengan Riska tapi saya akan menjawab kembali menurut saya dia cenderung menggunakan basa kuat supaya dapat memikat perhatian dari hidrogen asam dengan kuat. Nukleofil pada reaksi e2 ini dapat bertindak sebagai basa sehingga dia bisa mengambil Proton atau hidrogen dari atom karbon yang atom karbonnya berdekatan dengan karbon pengantar gugus pergi. Kemudian pada waktu yang sama, gugus pergi itu terbebas dan setelah itu ikatan rangkap dua pun mulai tersusun.
Itu lah jawaban dari saya
Semoga bisa membantu 🙏